引言
政策速递[烟花] 器审中心发布《关于创新医疗器械临床试验方案预审查有关事项的通知》[玫瑰] ——进一步规范与提升临床试验方案预审查工作效率
各有关单位:
为全面落实《关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》(国办发〔2024〕53号),进一步提高临床试验方案预审查工作效率,切实推动创新技术临床转化,现就临床试验方案预审查有关事项进一步明确如下:
一、申请人应通过器审中心开通的创新产品重大技术问题咨询沟通路径提出临床试验方案预审查申请,并在标题中明确此次申请为“×××(产品名称)临床试验方案预审查”。
二、申请人应确保在完成必要的非临床研究和临床试验可行性研究(必要时)的前提下提交临床试验方案预审查申请。临床试验方案应经过科学论证,并在充分考虑产品特征、临床风险和已有临床数据的基础上制定。
三、申请人应按照附件1、2的要求提交立题依据综述、必要的非临床研究资料、临床试验方案以及相关支持性资料。相关资料应能够阐明产品适用范围/预期用途、工作原理/作用机理/检验原理、结构组成/主要组成成分和材料信息(如适用)等,确认产品关键功能和性能参数,并充分证明预期临床风险可接受。
四、器审中心将对预审查申请的相关资料进行审核,如经审核认为提交资料不符合上述要求,审核部门可通过视频会议等方式将存在的问题及需要补充完善的研究资料反馈申请人,并告知申请人本次无法确认临床试验方案,待申请人按要求补充相关研究资料,并重新提出申请后,再行开展临床试验方案预审查;如经审核认为提交资料符合要求,则开展临床试验方案预审查,必要时可召开专家咨询会,申请人应配合开展相关工作,并在沟通交流和咨询会议中详细介绍产品设计开发及临床试验方案设计的基本情况。
五、器审中心基于现阶段科学认知或临床共识对临床试验方案或临床试验设计要求提出预审查意见,并以适当方式反馈申请人。建议申请人按照预审查意见开展临床试验,如有方案调整,需充分考虑由此增加的风险和不确定性。
六、如通过临床试验方案预审查后,产品设计或技术特征等发生显著变化(但不影响产品创新点的认可),建议重新进行临床试验方案预审查。
七、临床试验方案预审查意见为指导申请人科学开展临床试验设计提供服务,不作为技术审评意见和结论。
特此通知。
附件:
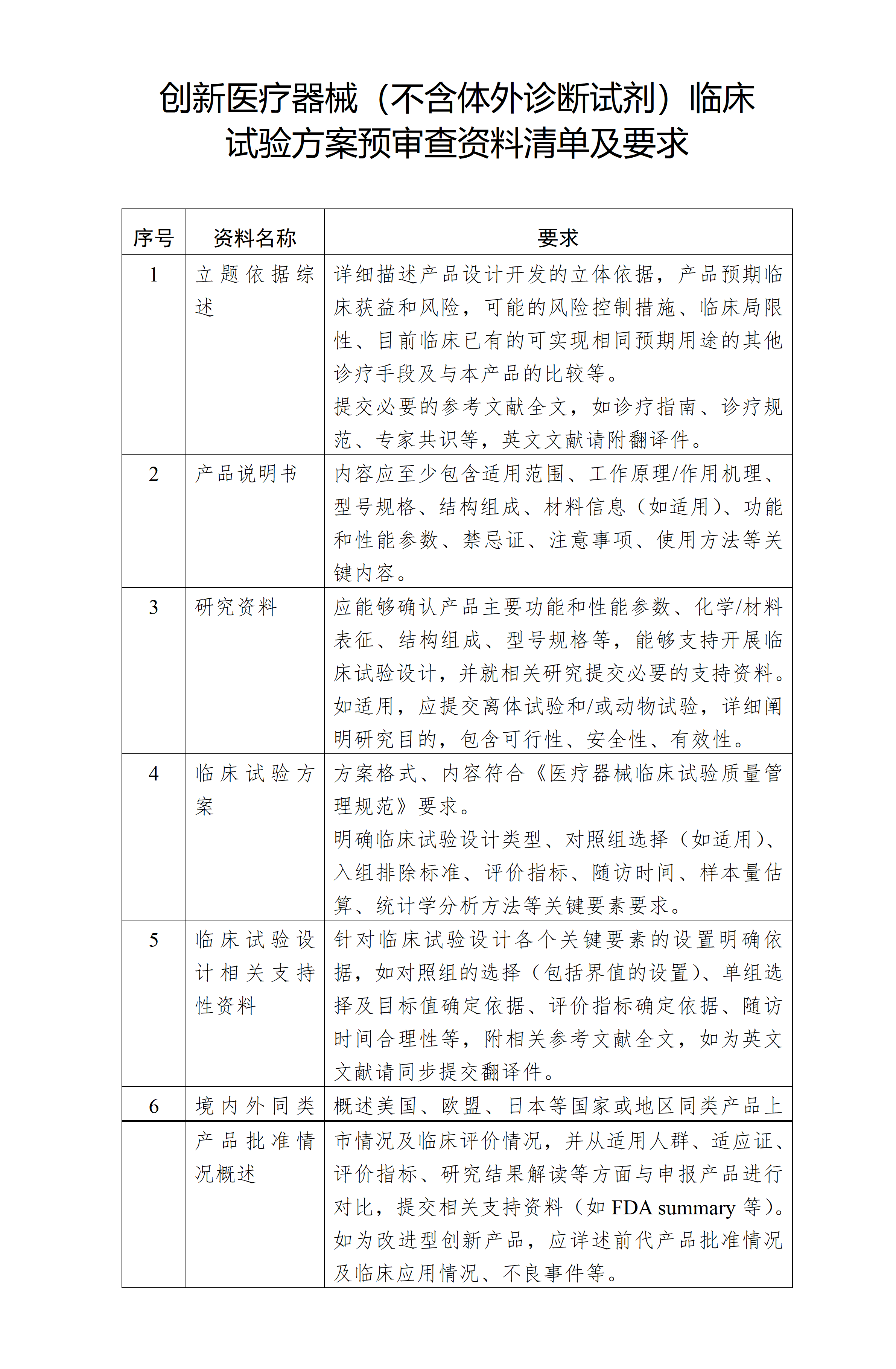
1.创新医疗器械(不含体外诊断试剂)临床试验方案预审查资料清单及要求
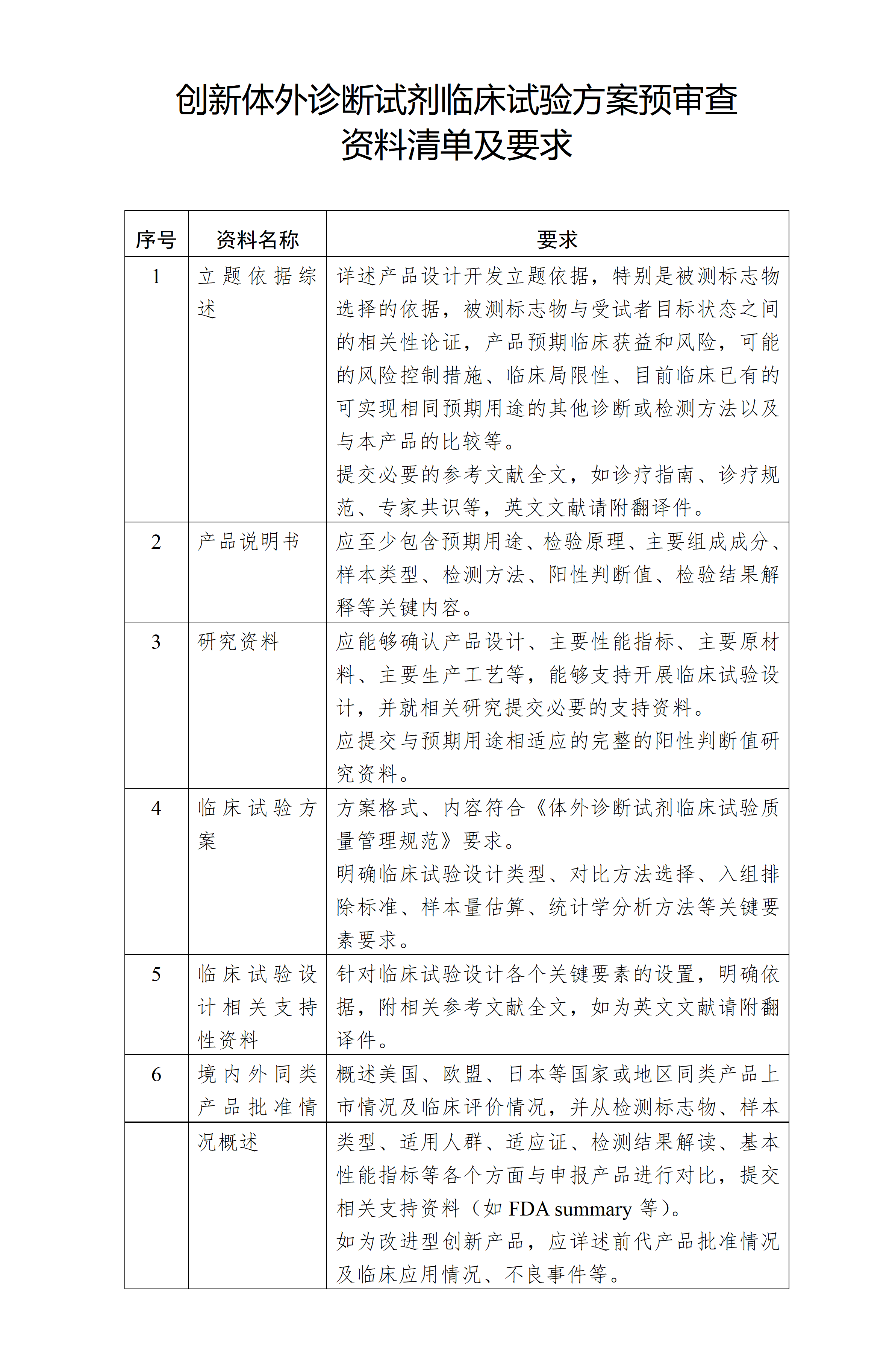
2.创新体外诊断试剂临床试验方案预审查资料清单及要求
国家药品监督管理局
医疗器械技术审评中心
2026年3月6日
附件1.创新医疗器械(不含体外诊断试剂)临床试验方案预审查资料清单及要求
附件2.创新体外诊断试剂临床试验方案预审查资料清单及要求